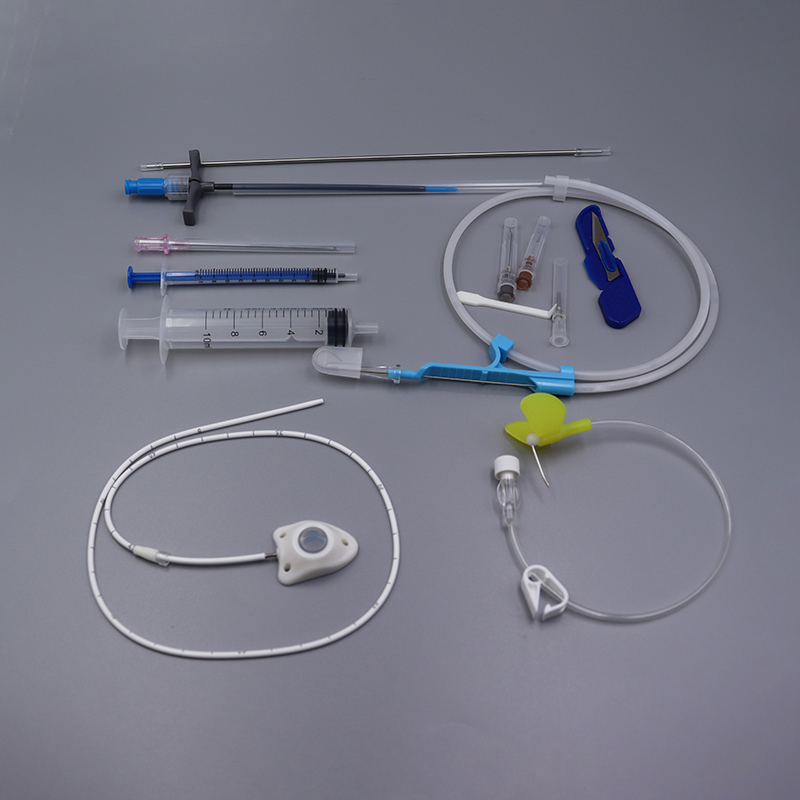
[Applicazione] Il dispositivo vascolareporta impiantabileè adatto per la chemioterapia guidata per una varietà di tumori maligni, per la chemioterapia profilattica dopo la resezione del tumore e per altre lesioni che richiedono una somministrazione locale a lungo termine.
[Specifiche]
| Modello | Modello | Modello |
| I-6,6 Fr×30 cm | II-6,6 Fr×35 cm | III- 12,6 Fr×30 cm |
【Prestazioni】L'elastomero autosigillante del supporto per iniezione consente agli aghi da 22 GA di una porta impiantabile di perforare 2000 volte. Il prodotto è realizzato interamente in polimeri medicali ed è privo di metallo. Il catetere è rilevabile ai raggi X. Sterilizzato con ossido di etilene, monouso. Design antireflusso.
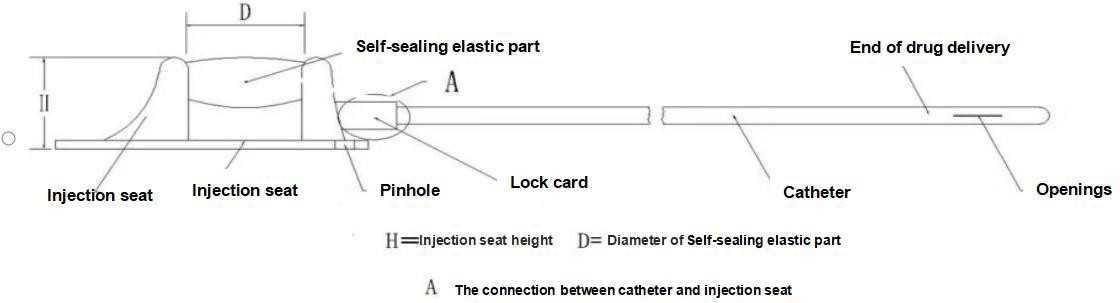
【Struttura】Questo dispositivo è costituito da una sede di iniezione (incluse parti elastiche autosigillanti, parti di restrizione della puntura, clip di bloccaggio) e un catetere, e il prodotto di Tipo II è dotato di un booster con clip di bloccaggio. Il catetere e la membrana elastica autosigillante del dispositivo impiantabile per la somministrazione di farmaci sono realizzati in gomma siliconica medicale e gli altri componenti sono realizzati in polisulfone medicale. Il diagramma seguente presenta la struttura principale e i nomi dei componenti del prodotto, considerando il tipo I come esempio.
【Controindicazioni】
1) Inidoneità psicologica o fisica all'intervento chirurgico in condizioni generali
2) Gravi disturbi emorragici e della coagulazione.
3) Conta dei globuli bianchi inferiore a 3×109/L
4) Allergia ai mezzi di contrasto
5) Combinata con grave broncopneumopatia cronica ostruttiva.
6) Pazienti con allergia nota o sospetta ai materiali presenti nella confezione del dispositivo.
7) Presenza o sospetto di infezione, batteriemia o sepsi correlata al dispositivo.
8) Radioterapia nel sito di inserimento previsto.
9) Imaging o iniezione di farmaci embolici.
【Data di fabbricazione】 Vedi etichetta del prodotto
【Data di scadenza】 Vedi etichetta del prodotto
【Metodo di applicazione】
- Preparare il dispositivo impiantabile e verificare che la data di scadenza sia stata superata; rimuovere la confezione interna e verificare che la confezione non sia danneggiata.
- Utilizzare tecniche asettiche per aprire la confezione interna ed estrarre il prodotto per prepararlo all'uso.
- L'uso dei dispositivi portuali impiantabili è descritto separatamente per ciascun modello come segue.
TipoⅠ
- Lavaggio, sfiato, prova di tenuta
Utilizzare una siringa (ago per dispositivo port impiantabile) per perforare il dispositivo port impiantabile e iniettare 5-10 ml di soluzione fisiologica per lavare la sede di iniezione e il lume del catetere ed escludere. Se non si trova liquido o il liquido è lento, ruotare manualmente l'estremità di erogazione del farmaco del catetere (estremità distale) per aprire la porta di erogazione del farmaco; quindi ripiegare l'estremità di erogazione del farmaco del catetere, continuare a spingere la soluzione salina (pressione non superiore a 200 kPa), osservare se ci sono perdite dalla sede di iniezione e dalla connessione del catetere, dopo che tutto è tornato alla normalità. Una volta che tutto è tornato alla normalità, il catetere può essere utilizzato.
- Cannulazione e legatura
In base all'indagine intraoperatoria, inserire il catetere (estremità di somministrazione del farmaco) nel vaso sanguigno corrispondente in base alla sede del tumore e utilizzare suture non assorbibili per legare correttamente il catetere al vaso. Il catetere deve essere legato correttamente (due o più passaggi) e fissato.
- chemioterapia e sigillatura
Il farmaco chemioterapico intraoperatorio può essere iniettato una volta secondo il piano di trattamento; si raccomanda di lavare la sede di iniezione e il lume del catetere con 6-8 ml di soluzione fisiologica, seguiti da 3 ml~5 ml. Il catetere viene quindi sigillato con 3-5 ml di soluzione salina eparina a 100 U/mL-200 U/mL.
- Fissaggio del sedile di iniezione
Si crea una cavità cistica sottocutanea in un punto di appoggio, a una distanza compresa tra 0,5 cm e 1 cm dalla superficie cutanea, e si posiziona e si fissa la sede di iniezione nella cavità, suturando la cute dopo un'emostasi rigorosa. Se il catetere è troppo lungo, può essere arrotolato a forma di cerchio all'estremità prossimale e fissato correttamente.
Tipo II
1. Lavaggio e sfiato
Utilizzare una siringa (ago per dispositivo port impiantabile) per iniettare soluzione salina rispettivamente nella sede di iniezione e nel catetere per lavare e rimuovere l'aria nel lume e osservare se il fluido di conduzione è liscio.
2. Cannulazione e legatura
In base all'indagine intraoperatoria, inserire il catetere (estremità di somministrazione del farmaco) nel vaso sanguigno corrispondente in base alla sede del tumore e legare correttamente il catetere al vaso con suture non assorbibili. Il catetere deve essere legato correttamente (due o più passaggi) e fissato.
3. Connessione
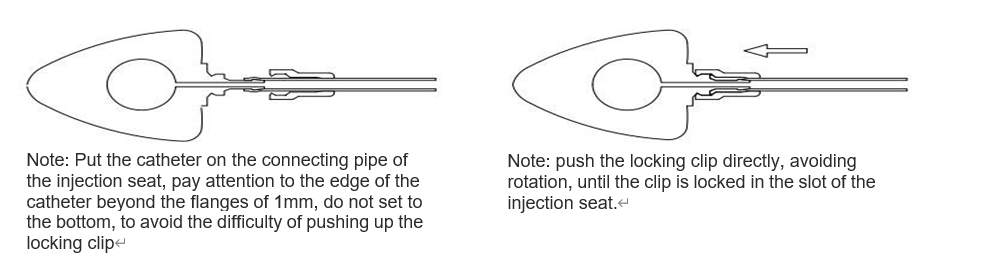
Determinare la lunghezza del catetere richiesta in base alle condizioni del paziente, tagliare l'eccesso dall'estremità prossimale del catetere (estremità non dosatrice) e inserire il catetere nel tubo di collegamento della sede di iniezione utilizzando
Utilizzare il booster per la clip di bloccaggio per spingere saldamente la clip di bloccaggio in modo che aderisca saldamente al supporto dell'iniezione. Quindi tirare delicatamente il catetere verso l'esterno per verificare che sia ben fissato. Questa operazione viene eseguita come mostrato in
Figura sotto.
4. Prova di tenuta
4. Dopo aver completato il collegamento, piegare e chiudere il catetere nella parte posteriore della clip di bloccaggio e continuare a iniettare la soluzione salina nella sede di iniezione con una siringa (ago per dispositivo di somministrazione di farmaci impiantabile) (pressione superiore a 200 kPa). (pressione non superiore a 200 kPa), osservare se vi sono perdite dal blocco di iniezione e dal catetere
connessione e utilizzarla solo dopo che tutto è tornato alla normalità.
5. Chemioterapia, sigillatura del tubo
Il farmaco chemioterapico intraoperatorio può essere iniettato una volta secondo il piano di trattamento; si consiglia di lavare nuovamente la base di iniezione e il lume del catetere con 6~8 ml di soluzione fisiologica e poi utilizzare 3~5 ml di soluzione fisiologica.
Il catetere viene quindi sigillato con 3-5 ml di soluzione salina di eparina a 100-200 U/ml.
6. Fissaggio della sede di iniezione
È stata creata una cavità cistica sottocutanea in un punto di appoggio, a 0,5-1 cm dalla superficie cutanea, e la sede di iniezione è stata posizionata nella cavità e fissata, e la pelle è stata suturata dopo una rigorosa emostasi.
Tipo III
È stata utilizzata una siringa (ago speciale per dispositivo impiantabile) per iniettare 10 ml ~ 20 ml di soluzione salina normale nel dispositivo impiantabile per la somministrazione del farmaco, per lavare la sede di iniezione e la cavità del catetere, rimuovere l'aria nella cavità e osservare se il fluido era discreto.
2. Cannulazione e legatura
In base all'esplorazione intraoperatoria, inserire il catetere lungo la parete addominale; la parte aperta dell'estremità di somministrazione del farmaco deve entrare nella cavità addominale e trovarsi il più vicino possibile al bersaglio tumorale. Scegliere 2-3 punti per legare e fissare il catetere.
3. chemioterapia, sigillatura del tubo
Il farmaco chemioterapico intraoperatorio può essere iniettato una volta secondo il piano di trattamento, quindi il tubo viene sigillato con 3 ml~5 ml di soluzione salina di eparina 100 U/mL~200 U/mL.
4. Fissaggio della sede di iniezione
È stata creata una cavità cistica sottocutanea in un punto di appoggio, a 0,5-1 cm dalla superficie cutanea, e la sede di iniezione è stata posizionata nella cavità e fissata, e la pelle è stata suturata dopo una rigorosa emostasi.
Infusione e cura dei farmaci
UN.Intervento rigorosamente asettico, corretta selezione della sede di iniezione prima dell'iniezione e rigorosa disinfezione del sito di iniezione.B. Durante l'iniezione, utilizzare un ago per dispositivo port impiantabile, una siringa da 10 ml o più, con l'indice della mano sinistra a contatto con il sito di puntura e il pollice che tende la pelle mentre fissa la sede di iniezione, con la mano destra che tiene la siringa verticalmente nell'ago, evitando di scuoterla o ruotarla, e iniettare lentamente 5 ml~10 ml di soluzione salina quando si avverte una sensazione di caduta e la punta dell'ago tocca successivamente il fondo della sede di iniezione, e verificare che il sistema di somministrazione del farmaco sia scorrevole (in caso contrario, verificare prima se l'ago è bloccato). Osservare se si verifica un sollevamento della pelle circostante durante la spinta.
C. Iniettare lentamente il farmaco chemioterapico dopo aver verificato che non vi siano errori. Durante l'iniezione, prestare attenzione a verificare se la pelle circostante è sollevata o pallida e se è presente dolore locale. Dopo l'iniezione, il farmaco deve essere mantenuto per 15-30 secondi.
D. Dopo ogni iniezione, si raccomanda di lavare la sede di iniezione e il lume del catetere con 6~8 ml di soluzione fisiologica, quindi sigillare il catetere con 3~5 ml di soluzione salina eparina 100U/mL~200U/mL; una volta iniettati gli ultimi 0,5 ml di soluzione salina eparina, il farmaco deve essere spinto durante la retrazione, in modo che il sistema di introduzione del farmaco sia riempito di soluzione salina eparina per prevenire la cristallizzazione del farmaco e la coagulazione del sangue nel catetere. Il catetere deve essere lavato con soluzione salina eparina una volta ogni 2 settimane durante l'intervallo di chemioterapia.
E. Dopo l'iniezione, disinfettare la cruna dell'ago con un disinfettante medico, coprirla con una medicazione sterile e fare attenzione a mantenere la zona interessata pulita e asciutta per prevenire infezioni nel sito di puntura.
F. Prestare attenzione alla reazione del paziente dopo la somministrazione del farmaco e osservare attentamente durante l'iniezione del farmaco.
【Attenzione, avvertenza e contenuto suggestivo】
- Questo prodotto è sterilizzato con ossido di etilene ed è valido per tre anni.
- Per garantire la sicurezza dell'uso, leggere attentamente il manuale di istruzioni prima dell'uso.
- L'uso di questo prodotto deve essere conforme ai requisiti dei codici di condotta e delle normative pertinenti del settore medico e l'inserimento, l'utilizzo e la rimozione di questi dispositivi devono essere riservati a medici certificati. L'inserimento, l'utilizzo e la rimozione di questi dispositivi sono riservati a medici certificati e l'assistenza post-inserimento del sondino deve essere eseguita da personale medico qualificato.
- L'intera procedura deve essere eseguita in condizioni asettiche.
- Prima della procedura, controllare la data di scadenza del prodotto e verificare che la confezione interna non sia danneggiata.
- Dopo l'uso, il prodotto può causare rischi biologici. Si prega di seguire le pratiche mediche accettate e tutte le leggi e i regolamenti pertinenti per la manipolazione e il trattamento.
- Non esercitare una forza eccessiva durante l'intubazione e inserire l'arteria con precisione e rapidità per evitare vasospasmo. Se l'intubazione risulta difficoltosa, utilizzare le dita per ruotare il catetere da un lato all'altro durante l'inserimento del tubo.
- La lunghezza del catetere inserito nel corpo deve essere adeguata: se troppo lungo, può facilmente piegarsi in un angolo, con conseguente scarsa ventilazione; se troppo corto, può causare il distacco del catetere dal vaso in caso di attività violente del paziente. Se il catetere è troppo corto, potrebbe distaccarsi dal vaso in caso di movimenti vigorosi del paziente.
- Il catetere deve essere inserito nel vaso con più di due legature e con la dovuta tensione per garantire un'iniezione fluida del farmaco e impedire che il catetere scivoli via.
- Se il dispositivo impiantabile è di tipo II, la connessione tra il catetere e la sede di iniezione deve essere salda. Se non è necessaria l'iniezione intraoperatoria del farmaco, è necessario effettuare un'iniezione di prova con soluzione fisiologica per conferma prima di suturare la cute.
- Quando si separa la zona sottocutanea, è necessario eseguire un'emostasi accurata per evitare la formazione di ematomi locali, accumulo di liquidi o infezioni secondarie dopo l'intervento chirurgico; la sutura vescicolare deve evitare la sede di iniezione.
- Gli adesivi medicali a base di α-cianoacrilato possono danneggiare il materiale della base di iniezione; non utilizzare adesivi medicali a base di α-cianoacrilato durante il trattamento dell'incisione chirurgica attorno alla base di iniezione. Non utilizzare adesivi medicali a base di α-cianoacrilato durante il trattamento di incisioni chirurgiche attorno alla base di iniezione.
- Prestare la massima attenzione per evitare perdite del catetere dovute a lesioni accidentali causate da strumenti chirurgici.
- Durante la puntura, l'ago deve essere inserito verticalmente, deve essere utilizzata una siringa con una capacità di 10 ml o superiore, il farmaco deve essere iniettato lentamente e l'ago deve essere estratto dopo una breve pausa. La pressione di spinta non deve superare i 200 kPa.
- Utilizzare solo aghi speciali per dispositivi impiantabili per la somministrazione di farmaci.
- Quando è necessaria un'infusione più lunga o la sostituzione del farmaco, è opportuno utilizzare un dispositivo di somministrazione del farmaco impiantabile monouso con ago per infusione speciale o raccordo a T, per ridurre il numero di punture e l'impatto sul paziente.
- Ridurre il numero di punture, ridurre i danni ai muscoli del paziente e alle parti elastiche autosigillanti. Durante il periodo di sospensione dell'iniezione di farmaci, è necessaria un'iniezione di anticoagulante una volta ogni due settimane.
- Questo prodotto è monouso, sterile, apirogeno, va distrutto dopo l'uso e il riutilizzo è severamente vietato.
- Se la confezione interna è danneggiata o è stata superata la data di scadenza del prodotto, restituirlo al produttore per lo smaltimento.
- Il numero di forature per ogni blocco di iniezione non deve superare 2000 (22Ga). 21.
- Il volume minimo di lavaggio è 6 ml
【Magazzinaggio】
Questo prodotto deve essere conservato in un ambiente non tossico, non corrosivo, ben ventilato e pulito, evitandone l'estrusione.
Data di pubblicazione: 25-03-2024