Indicazioni per l'uso (descrivere)
Microsfere embolichesono destinati ad essere utilizzati per l'embolizzazione di malformazioni arterovenose (MAV) e tumori ipervascolarizzati, compresi i fibromi uterini.
Nome comune o usuale: Classificazione delle microsfere emboliche di alcol polivinilico
Nome: Dispositivo per embolizzazione vascolare
Classificazione: Classe II
Pannello: Cardiovascolare
Descrizione del dispositivo
Le microsfere emboliche sono microsfere di idrogel comprimibili con forma regolare, superficie liscia e dimensioni calibrate, ottenute tramite modificazione chimica di materiali a base di alcol polivinilico (PVA). Le microsfere emboliche sono costituite da un macromero derivato dall'alcol polivinilico (PVA), sono idrofile, non riassorbibili e disponibili in diverse dimensioni. La soluzione di conservazione è una soluzione di cloruro di sodio allo 0,9%. Il contenuto di acqua delle microsfere completamente polimerizzate è compreso tra il 91% e il 94%. Le microsfere possono sopportare una compressione del 30%.
Le microsfere emboliche vengono fornite sterili e confezionate in fiale di vetro sigillate.
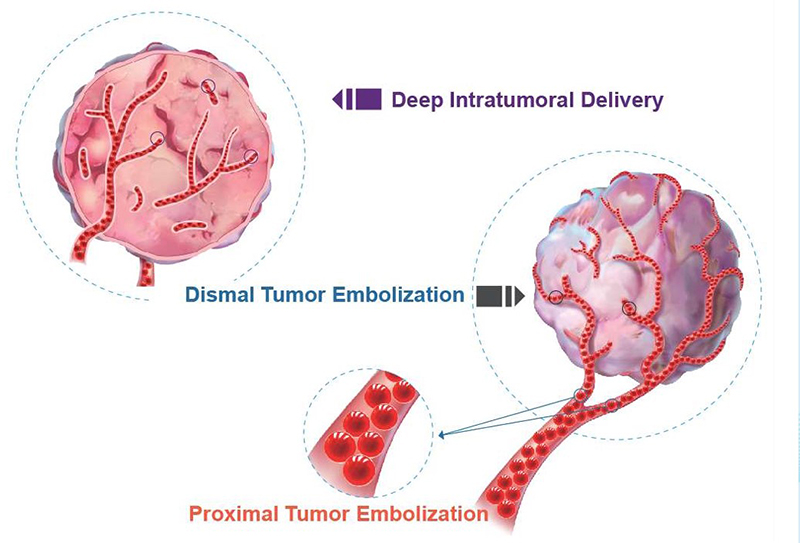
Le microsfere embolizzanti sono destinate all'embolizzazione di malformazioni arterovenose (MAV) e tumori ipervascolarizzati, inclusi i fibromi uterini. Bloccando l'afflusso di sangue all'area interessata, il tumore o la malformazione vengono privati dei nutrienti e si riducono di dimensioni.
Le microsfere emboliche possono essere somministrate tramite microcateteri standard di calibro compreso tra 1,7 e 4 Fr. Al momento dell'uso, le microsfere emboliche vengono miscelate con un mezzo di contrasto non ionico per formare una soluzione in sospensione. Le microsfere emboliche sono monouso e fornite sterili e apirogene. Le configurazioni del dispositivo per la somministrazione di microsfere emboliche sono descritte nelle Tabelle 1 e 2 riportate di seguito.
Tra le varie gamme dimensionali delle microsfere embolizzanti, quelle utilizzabili per l'embolizzazione dei fibromi uterini sono 500-700 μm, 700-900 μm e 900-1200 μm.
| Tabella: Configurazioni del dispositivo delle microsfere emboliche | ||||
| Prodotto Codice | Calibrato Dimensione (µm) | Quantità | Indicazione | |
| Tumori ipervascolari/arteriovenosi Malformazioni | Fibroma uterino | |||
| B107S103 | 100-300 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| B107S305 | 300-500 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| B107S507 | 500-700 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| B107S709 | 700-900 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| B107S912 | 900-1200 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| B207S103 | 100-300 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| B207S305 | 300-500 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| B207S507 | 500-700 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| B207S709 | 700-900 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| B207S912 | 900-1200 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| Prodotto Codice | Calibrato Dimensione (µm) | Quantità | Indicazione | |
| Tumori ipervascolari/arteriovenosi Malformazioni | Fibroma uterino | |||
| U107S103 | 100-300 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| U107S305 | 300-500 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| U107S507 | 500-700 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| U107S709 | 700-900 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| U107S912 | 900-1200 | 1 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| U207S103 | 100-300 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| U207S305 | 300-500 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | No |
| U207S507 | 500-700 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| U207S709 | 700-900 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
| U207S912 | 900-1200 | 2 ml di microsfere : 7 ml 0,9% cloruro di sodio | SÌ | SÌ |
Data di pubblicazione: 27 febbraio 2024